うつ病治療におけるMeasurement-Based Care ―現在と未来―【学会共催シンポジウム】
座長:中川 伸 先⽣(山口大学大学院医学系研究科高次脳機能病態学講座)
岸本 泰士郎 先⽣(慶應義塾大学医学部ヒルズ未来予防医療・ウェルネス共同研究講座)
講演1
うつ病診療における認知機能障害評価の現状と課題
堀 輝 先生(福岡大学医学部精神医学教室)
精神科診療におけるMeasurement-Based Careと認知機能障害
精神科診療において、精神症状の定量化が困難であることや不十分であることが課題となっている。そこで現在注目されているのがMeasurement-Based Care (MBC)である。MBCの実践により、症状の定量化、診療におけるEvidence-Based Medicine (EBM)、Shared Decision Making (SDM)への利用、症状モニタリングによる個別化治療、治療反応の見極め、患者の治療参加への促進がもたらされ、より早期の寛解が期待されると考えられる。Canadian Network for Mood and Anxiety Treatments (CANMAT)による成人うつ病(MDD)ガイドライン2023年版ではMBCの実践に有用な検証済みの評価スケールが紹介されており、医療者評価による客観スケールとしてHAM-DやMADRS、C-SSRSなど、患者評価による自記式スケールとしてBDI、PHQ-9、QIDS-SR、CUDOSなどが挙げられているほか、近年重要視されているリカバリーの観点から、機能やQOL、副作用などの評価スケールも挙げられている1。
認知機能とは、記憶力、注意・集中力などの基本的な知的能力に加えて、計画、思考、判断、実行、問題解決などの複雑な知的能力を指す。この認知機能が障害されることで日常生活や社会活動全般に支障を来し、作業能力の低下や融通がきく行動がとれなかったり、複雑なことや新しいことを覚えることが困難になったりする。認知機能障害と気分障害には関連性があり、多くの気分障害患者では客観的評価で認知機能障害が存在すること2,3、MDDが寛解しても約半数で認知機能障害が残存しており再発のリスクになること4、認知機能障害は職業機能や対人関係機能と関連することが報告されている5。認知機能は、記憶と学習、作動記憶、注意・集中、遂行機能、処理速度などの神経認知機能ドメインに分類されるが6、近年は社会認知機能の重要性も指摘されている。
うつ病診療における認知機能評価の課題
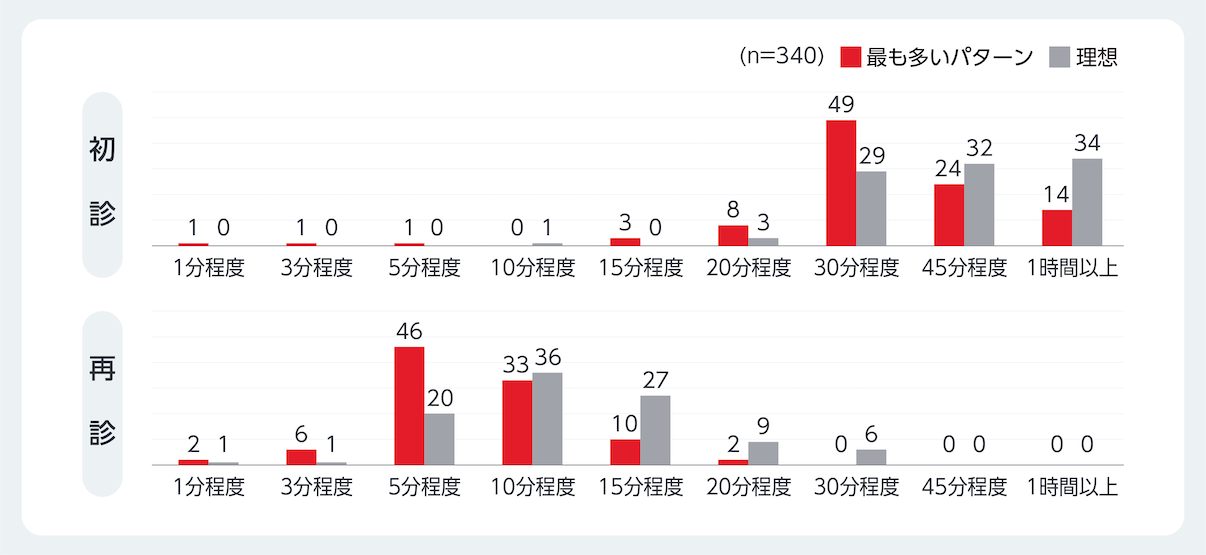
本邦の精神科医340人を対象にうつ病の診療課題に関するアンケート調査を行った結果、理想の初診時間は1時間以上が最も多かった一方で、実際の初診時間は30分程度が最も多かった。同様に、理想の再診時間は10分程度、15分程度の順に多かったが、実際は5分程度が最も多かった(図1)。うつ病診断時、80%以上の医師がほぼ全例に対し精神疾患の既往歴、睡眠の状態、生活歴など問診による確認を行っていたのに対し、心理検査をほぼ全例に実施していたのは19%程度であった。また、うつ病の臨床課題について「うつ病による認知機能障害の改善は復職の重要な要因である」に84%が同意していたが、実際に評価尺度を用いて評価を行っている医師の割合は多くなく、簡便とされるDSST課題については知られておらず、全く評価もされていないという現状であった 7。
うつ病患者と医療者の認識に関する研究では、急性期では精神症状、身体症状、認知機能障害のいずれも両者で認識は一致していた。しかし、復職時は認知機能障害の改善が重要と理解されているにも関わらず寛解期において医療者は患者の症状を低く見積もりがちであり、両者の認識にずれがあることが示された8。うつ病の神経心理学的症状のパターンは多様であり、実際に評価しないと患者の認知機能の障害度は判定できない。また、患者の主観的な認知機能障害は客観的な認知機能障害と相関しないことも報告されている9。
そこで大事なのが、日常診療で認知機能について話題にすること、すなわち、図2のような質問を実生活の場面をイメージしながら患者に聞くことである。そして認知機能障害の疑いがある場合は、診察室で5分以内に評価可能なDSST課題(職場、学校、家庭における機能レベルと相関)の実施を提案する10。また、待合室における待ち時間を利用して、自記式のPDQ-5やCOBRA、THINC-it®課題などを使用することも有用であろう。さらに、精査が必要な場合にはMCCBや簡易認知機能評価バッテリー(BAC-A)などの精密な神経心理学的検査に移行する。一方で、認知機能評価やMBCが広まらない要因としてコストとリソースの問題が挙げられる。今後は簡便かつ有用な神経心理検査を整備し、そこに診療報酬を反映させることも重要であると考えられる。
図1 アンケート結果:理想および実際の初診時間と再診時間
【対象/方法】2018年1月15~29日に、過去1ヵ月間にうつ病患者30名以上を治療した精神科又は心療内科専門医340名(男性90%、精神科所属95%、病院勤務医73%)を対象に、診療に関する実態調査(インターネット調査)を実施し解析した。アンケートは28項目から構成され、医師の経歴やうつ病の診断基準、診断ツールなどについて質問した。アンケート全体で2分以内に完了した回答者及びいくつかの質問に対する回答が同一の回答者は除外した。
【Limitation】本調査は既存のオンラインパネルを使用したインターネット調査であり、質問票のデザインや回答者の回答状況により、系統的バイアスや無作為分散が生じた可能性がある。回答者の90%が男性医師であったことなどから、今回の結果が日本のうつ病治療の実態を十分には反映できていない可能性がある。
図2 認知機能に関する日常生活の状況を聴取する5つの質問
HAM-D:Hamilton Rating Scale for Depression.
MADRS:Montgomery Asberg Depression Rating Scale.
C-SSRS:Columbia-Suicide Severity Rating Scale.
BDI:Beck Depression Inventory.
PHQ-9:Patient Health Questionnaire-9.
QIDS-SR:Quick Inventory of Depressive Symptomatology-Self Report.
CUDOS:Clinically Useful Depression Outcome Scale.
DSST:Digit Symbol Substitution Test.
PDQ-5:Perceived Deficits Questionnaire-5 item.
COBRA:Cognitive complaints in bipolar disorder rating assessment.
THINC-it®:THINC-integrated tool.
MCCB:MATRICS Consensus Cognitive Battery.
BAC-A:Brief Assessment of Cognition In Affective Disorders.
講演2
Person-centeredなケアを目指すためのMBCの可能性:QOLやパーソナルリカバリーに注目して
越川 陽介 先生(関西医科大学医学部精神神経科学講座)
パーソナルリカバリーとMBC
パーソナルリカバリーとは、病気による制約があっても満足し、希望を持ち人生を送る道程であり、個人的で独特なプロセスである11。うつ病においては、罹患したことに対して自分なりの意味を見出し、これまでの過程を包括的に捉えて希望にあふれた生き方を主体的に模索することが重要である12。一方で、パーソナルリカバリーは個別性が高く言語化が困難であり、ゴールが個々で異なることから可視化が必要になる。
治療を通して収集されたクライエントのデータに基づいて臨床ケアを行う実践がMBCである13。MBCでは、患者のデータを日常的に収集し、タイムリーに患者にフィードバックを共有して治療参加を促すこと、すなわちデータに基づいた医療提供者の臨床的判断と患者の経験を両軸として行動することが重要である。CANMATによる成人MDDガイドラインでは、うつ病の様々な転帰を最適化する要素としてMBCが挙げられており14、症候学的リカバリーのみならず、機能的リカバリー、社会的リカバリー、パーソナルリカバリーにおいてもMBCの実践は必要であると考えられる。
パーソナルリカバリーにおいてMBCは、「現状の把握」、「患者のパーソナルリカバリーの発見」、「ゴールの具体化」に活用できると考えられる。「現状の把握」に利用可能な尺度がRASやQPRである。RASは24項目、QPRは22項目から成る自己記入式の尺度であり、パーソナルリカバリーに関する尺度の中で妥当性や信頼性において最も強いエビデンスを有している15。「パーソナルリカバリーの発見」で利用可能な尺度がSEIQoL-DWである。SEIQoL-DWは半構造化面接を用いたQOLの評価尺度であり、健康に問題を抱えながらも生活において重要だと感じている領域をQOLの評価に反映させることが可能である16。経時的な変化の理解にも有用であり17、評価の過程で新たな価値観や生きがいが生まれる可能性があることから18、患者本人にパーソナルリカバリーを考えてもらうきっかけになり得る19。そして「ゴールの具体化」に利用可能な尺度がGAS-Dである。GASは精神保健領域の評価のために提案された尺度で20、患者個別の問題を特定して適切なゴールを患者本人と検査者で協議しながら決定する21。2019年にうつ病に適応したGAS-Dが登場しており、GAS-Dでは明確な目標設定を行うためにSMART(Specific[具体的]、Measurable[測定可能]、Attainable[達成可能]、Realistic[現実的]、Time-bound[一定期間])目標を使用する22。たとえば図3のようなSMART目標を設定することで、設定した目標の達成度合を定量的に評価することが可能になり、患者自身も達成状況を理解しやすくなる。
パーソナルリカバリーのためのはじめの一歩 -フォーカシングの観点から-
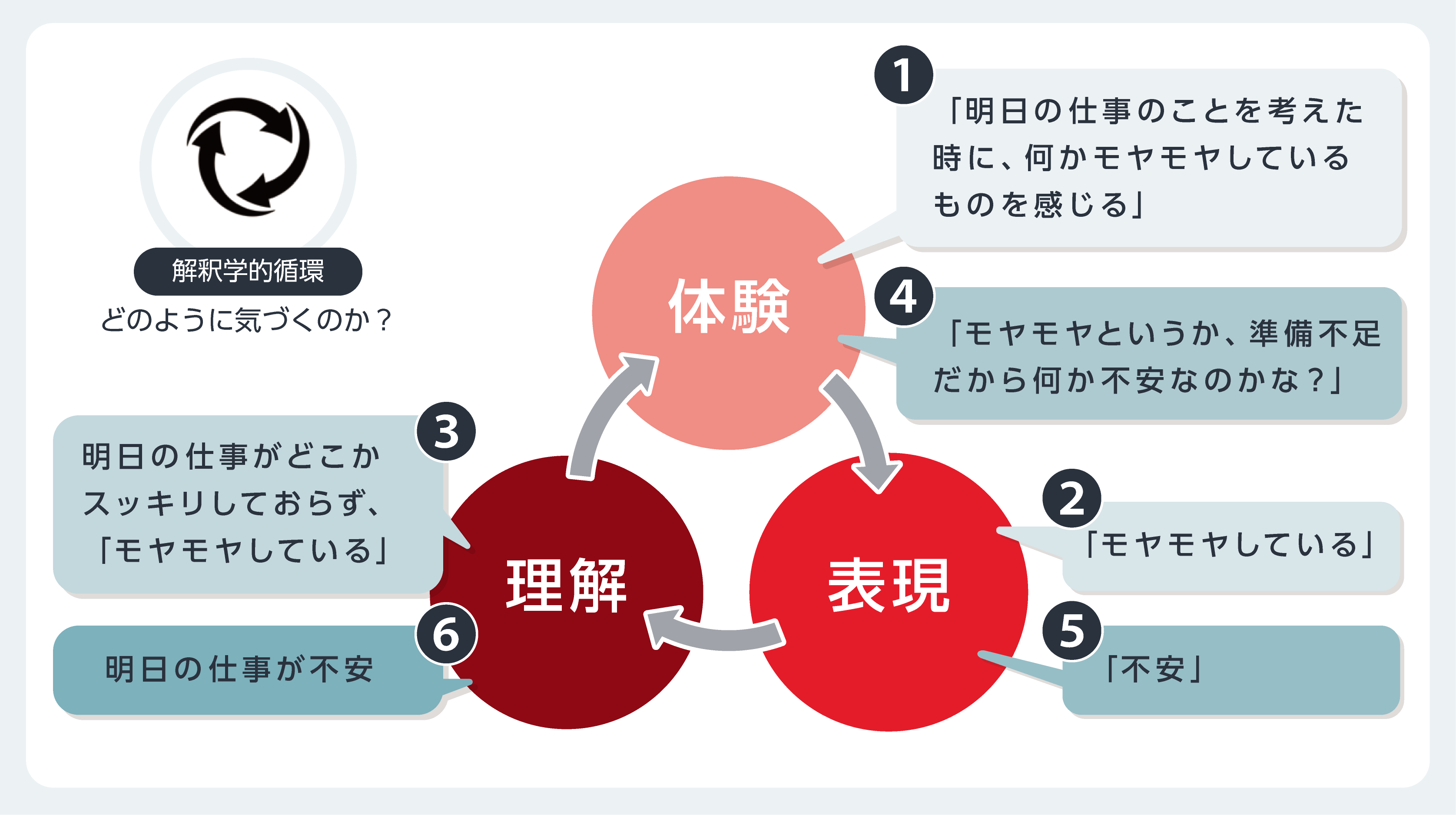
パーソナルリカバリーを取り扱うことの困難さのひとつに、何がパーソナルリカバリーに繋がるのかが分かりにくい点が挙げられ、これは尺度を使用しても回答は得られない。個別性が高いパーソナルリカバリーを達成するためには患者の自己理解が求められ、その手法の一つとしてフォーカシングが役に立つと考えられる。フォーカシングとは、漠然としていて言語で明確に説明することが困難な感覚に注意を向けて、それを言語化することを手掛かりに自分自身を理解していく過程である23。パーソナルリカバリーの過程は個別性が高いため、本人が主体的に生き方を模索することが重要であり、そのためには自己への気づきが必要になる。気づきには「何に気づくのか」「どのように気づくのか」の2つの側面がある。前者では体験に伴う身体感覚を活用して、自分にとっての充実した生活や体験についての「感じ」に触れ、取り上げた目標がしっくりきているかを問いかける。このことは、自分の行動や目標を決める指針となる。後者では自己理解を促進させ自分を知るために、図4のように体験、表現、理解の解釈学的循環を活用する。このように自己理解が進展するプロセスを追うことがフォーカシングであり、パーソナルリカバリーの発見と言語化に活用できると考えられる。
図3 SMARTの視点を用いた目標設定
図4 解釈学的循環と心理療法
池見陽, 編著. ほか.『傾聴・心理臨床学アップデートとフォーカシング 感じる・話す・聴くの基本』. 2016, ナカニシヤ出版, 京都府.
RAS:Recovery Assessment Scale.
QPR:Questionnaire about the Process of Recovery.
SEIQoL-DW:Schedule for the Evaluation of Individual Quality of Life-Direct Weighting.
GAS-D:Goal Attainment Scale for Depression.
講演3
デジタルフェノタイプを用いたうつ病定量技術の試み
岸本 泰士郎 先⽣(慶應義塾大学医学部ヒルズ未来予防医療・ウェルネス共同研究講座)
PROMPTプロジェクト-デジタル技術を用いた新しいうつ病診療へのアプローチ-
近年、ウェアラブルデバイスなどがインターネットに繋がることで、患者に負担をかけることなく生体情報の観察が可能となり、得られたビッグデータを機械学習で解析するなど、デジタル技術を用いた新しいアプローチが活発に行われている。そして、デジタルフェノタイピングは「個人用デジタル機器のデータを用いて個人レベルの表現型をその時点ごとに定量化すること」と定義されている24。我々は10年前から、うつ病患者の表情や音声、日常生活活動などの定量化による精神症状の客観的評価技術の開発を目指してProject for Objective Measures using computational Psychiatry Technology(PROMPT)プロジェクトに取り組んでいる。本プロジェクトの結果を3つ紹介する。
1つ目は、人工知能により患者の関節を推定して面接中の患者の体動を定量化した結果、うつ病患者は健常者と比較して体動速度が緩徐であることが確認され、うつ病の重症度評価との間に一定の相関が認められた(κ係数0.37-0.43)25。
2つ目は、話速及び反応時間を計測するソフトウェアを開発して話速などについて定量化した結果、うつ病の重症度は話速、反応速度、休止時間と相関することが示された(r=-0.378, r=0.298, r=0.458)26。
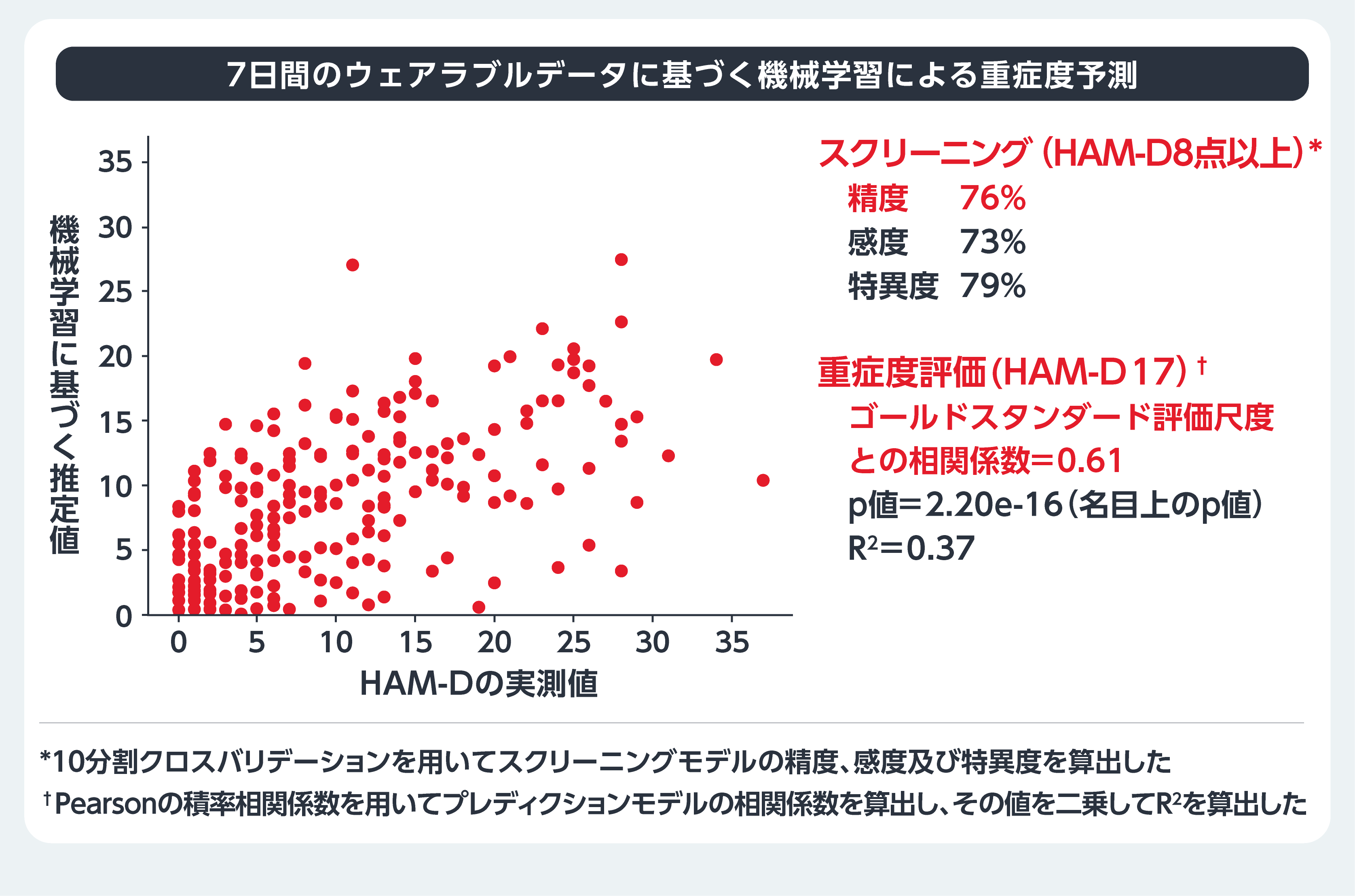
3つ目は、3軸加速度及び皮膚温、心拍、脈拍を定量可能なリストバンド型ウェアラブルデバイスを使用して体動、睡眠などを定量化し、うつ病の症状の有無(HAM-D17: 8点以上又は未満)を推定するスクリーニングモデル、及び重症度(HAM-D17の点数)を推定するプレディクションモデルを作成した27。機械学習のアプローチには解析結果を客観的に示すことが可能であるXGBoostを使用し、Feature Importanceと呼ばれる、重要視された特徴量に関する指標を付加することで、解釈可能な学習モデルを作成・検討している。本プロジェクトのパイロット研究では、うつ病患者と双極性障害患者合わせて45例、健常者41例がウェアラブルデバイスを装着して、入院患者は1~2週間ごと、外来患者は受診ごとに複数回精神症状のデータを取得した。解析の結果、スクリーニングの精度(HAM-D 8点以上か否か)は76%であり、重症度予測の相関係数は0.61であった(図5)27。また、Feature Importanceについて解析した結果、スクリーニング及び重症度予測のいずれにおいても活動量や睡眠だけではなく就寝時の皮膚温や心拍がより重要視されていた。
プロジェクトの展望と解決しうる臨床課題
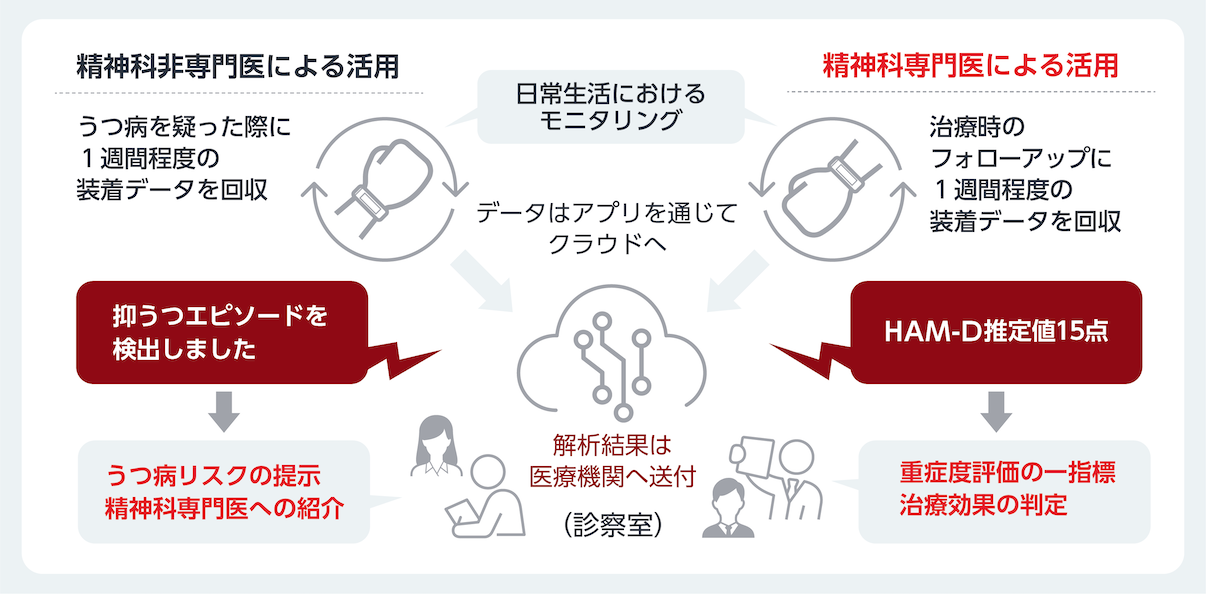
この3つ目のプロジェクトは日本医療研究開発機構(AMED)から評価され、本格的な医療機器としての開発が進行中である。精神科非専門医を受診した身体不定愁訴を抱えたうつ病患者に対する抑うつエピソードリスクの推定、又は専門医の再診患者における重症度評価の指標としての使用を想定しており、産学連携で患者データ収集、機械学習モデル構築、システム及び臨床開発、薬事申請の準備を進めている(図6)28。PROMPTプロジェクトの拡大版であるSWIFTプロジェクトでは、うつ病患者、健常者、そして不安症又は身体不定愁訴を抱えて内科受診した患者を対象とし、ウェアラブルデバイスを1週間装着して最大5回データを収集して最終日に評価した。そして今回は精神科診断面接マニュアル(SCID-5)を用いて抑うつエピソードの基準を満たすかの評価、HAM-Dによる重症度評価を行った。2024年5月時点で222例、743のデータセットが収集されている。
本邦におけるプログラム医療機器の開発の遅延を解消するために、厚生労働省はプログラム医療機器の優先審査指定制度を開始しており、本プロジェクトはその第1号に選定されている。うつ病の診断一致率は非常に低く、米国におけるSCID-5でもκ係数0.28である29。うつ病は生物学的指標が存在しないため、治療開始基準が不明確であり、治療反応が分かりにくく、新薬開発が困難であるなど様々な問題を抱えている。現在開発中の医療機器により、スクリーニングや重症度評価だけでなく、患者の層別化や治療提案、治療反応予測、そして医療情報の非対称性の解消にも役立てられればと考えている。患者が自身の状態をしっかり理解し、医療を選んでいく時代において、このような技術は患者のエンパワーメントの一助になると考え、開発を行っている。
図5 ウェアラブルデバイスを用いた重症度予測
図6 ウェアラブルデバイスを用いたうつ病診断支援技術開発・製品コンセプト
Kishimoto T, et al, Front Psychiatry, 2022, 13, 1025517作図
HAM-D:Hamilton Rating Scale for Depression
XGBoost:eXtreme Gradient Boosting.
SCID-5:Structured Clinical Interview for DSM-5.
パネルディスカッション
うつ病治療におけるMeasurement-Based Care
うつ病の多様な症状をいつ、どのように計測するか
堀 日常診療にMeasurementの文化が根付いていないため、まず実際にMeasurementしてみることが重要であり、そのためには心理士など多職種の協力が必要になります。現在、認知機能においては回復後に残存する機能障害を確認することはできるが、将来的にはプログラム医療機器などにより、予防や早期発見、急性期における機能障害の確認も可能になることを期待しています。
越川 急性期では今の辛さを解決してほしいというニーズが強く、パーソナルリカバリーを考慮する余裕はないため、パーソナルリカバリーは急性期の症状が落ち着いた後に評価を実施することになります。一方、待ち時間を利用したQIDS-SRなどの評価は最初から実施すべきであり、日常的に自分の症状を評価することが標準となると良いと考えています。
岸本 自己評価尺度でも標準的な評価でもMeasurementの文化が日本の精神医療に根付いてほしいと思います。現在はウェアラブルデバイスを使用している患者さんも多く、経過の可視化は患者さんも望んでいることが多いため、Measurementする医療を実践していければと思います。一方、評価の時間がないこと、尺度が標準化されておらず何を信じれば良いか分かりにくいことは問題であると考えています。
MBC実施による患者さんおよび家族へのメリット・デメリット
堀 Measurementにより重症度や治療反応を患者さんおよび家族と共有し、治療の必要性などを伝えることが可能になります。うつ病は多様な集団であるが、医療者が共通の評価をすることで患者さんにも医療者と共通の根拠を持たせることができるようになると考えています。
越川 視覚化が最大のメリットだと考えています。実際に臨床では目に見えないものを取り扱い、言葉でやり取りを行いますが、それだけでは記録は残りません。Measurementの実施により視覚的に経時的な推移を確認できるようになり、患者さんおよび家族の安心にもつながると思います。
岸本 デジタルテクノロジーを用いて患者さんの様子を観察すること自体に患者さんは非常に喜んでくださっていると感じており、客観的にみられることによって、患者さん、そしてご家族に対して、「医師が一生懸命患者さんを分かろうとしている」ことを伝えられるのではと思います。現在はオブジェクティブマーカーを創出することに注力していますが、一方で患者さんの主観を無視することがないよう、両者を組み合わせることも重要だと考えています。
中川 現在はHAM-DやMADRSなどの古典的な症状評価に、認知機能の新たな視点の評価が加わってきています。評価尺度を使用することは研究色が強いものでしたが、これからはこれらを融合させ、労力を割くことなくMeasurementすることが臨床上でも重要になってくると思われます。今後うつ病治療も新たなステップに入れるのではないかと期待しています。本日はありがとうございました。
QIDS-SR:Quick Inventory of Depressive Symptomatology-Self Report.
HAM-D:Hamilton Rating Scale for Depression.
MADRS:Montgomery Asberg Depression Rating Scale.